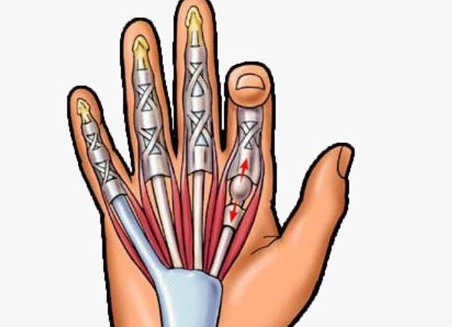
在手部疾病的临床诊疗中,屈指肌腱腱鞘炎(俗称 “扳机指”)与腕管综合征(Carpal Tunnel Syndrome, CTS)的共病现象日益受到关注。临床数据显示,扳机指患者中约 30%-40% 存在正中神经电生理异常表现,而类风湿关节炎患者中腕管综合征的发生率可高达 70%。这种高并发率揭示了两种疾病间存在深层病理联系,而非偶然巧合。本文将从解剖学基础、病因机制、病理联动及临床启示四个维度,系统阐述二者的关联本质,为临床诊疗提供理论依据。
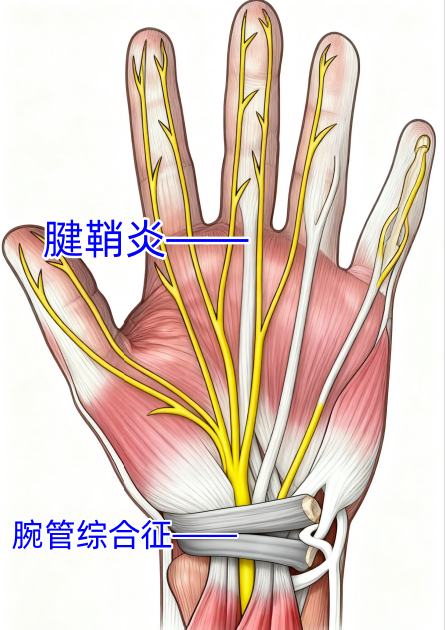
一、解剖学基础:腕管空间的精密平衡系统
腕管作为手部解剖的关键结构,是由腕骨构成的骨性底壁与腕横韧带形成的纤维性顶壁共同围成的密闭通道。这一解剖空间内包含 9 条屈指肌腱(拇长屈肌腱 1 条,指浅、深屈肌腱各 4 条)及正中神经,呈现 “肌腱 – 神经” 紧密并行的解剖关系。正常情况下,腕管内组织间维持着精准的空间配比,任何结构的体积异常增大都可能打破这种平衡。
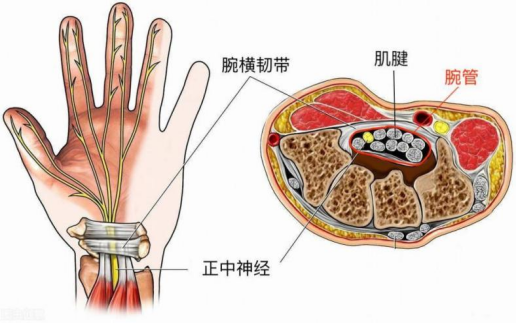
当屈指肌腱腱鞘炎发生时,腱鞘因反复机械刺激出现无菌性炎症反应,表现为滑膜细胞增生、纤维组织沉积及腱鞘增厚,形成 “动态占位病变”。这种病理改变使腕管内容物体积增加,在刚性骨纤维管道的限制下,腕管内压力呈指数级升高。研究表明,腕管内压力超过 30mmHg 时即可显著影响正中神经的微循环,导致神经轴浆运输障碍。值得注意的是,约 10%-15% 的人群存在永存正中动脉等解剖变异,这些变异血管会进一步减少腕管内代偿空间,使此类人群在发生腱鞘炎时更易出现正中神经卡压。
正中神经在腕管内的解剖位置使其成为最易受压迫的结构。该神经负责拇指、食指、中指及环指桡侧半的感觉与运动功能,受压后首先表现为感觉纤维传导障碍,出现麻木、刺痛等症状,随病情进展可累及运动纤维,导致拇短展肌等鱼际肌萎缩。这种 “空间侵占 – 功能障碍” 的直接关联,构成了两种疾病共病的解剖学基础。
二、共同病因:慢性劳损与系统性疾病的双重驱动
屈指肌腱腱鞘炎与腕管综合征的共病现象源于相似的病因学基础,可概括为慢性劳损与系统性疾病两大核心驱动因素。这两种疾病如同 “同源异流” 的病理过程,在相似的致病因素作用下,通过不同解剖靶点表现出临床症状。


慢性劳损作为最常见病因,通过机械力学机制同时影响肌腱和神经结构。长期重复性手部活动(如键盘操作、手工编织等)使屈肌腱与腱鞘之间产生持续摩擦,导致腱鞘组织出现充血、水肿、纤维化等一系列适应性改变,这是腱鞘炎的典型病理进程。与此同时,腕部反复屈伸动作会导致腕管内压力周期性升高,研究显示长期腕部过度使用可使腕管基础压力从正常的 2-5mmHg 升至 15-20mmHg,这种慢性高压状态会破坏正中神经的血 – 神经屏障,引发神经内水肿和脱髓鞘改变。一位每日键盘操作超过 8 小时的文员案例显示,其屈肌腱鞘厚度较正常人群增加 2.3 倍,同时伴有正中神经传导速度减慢 30%,生动体现了慢性劳损的双重致病作用。
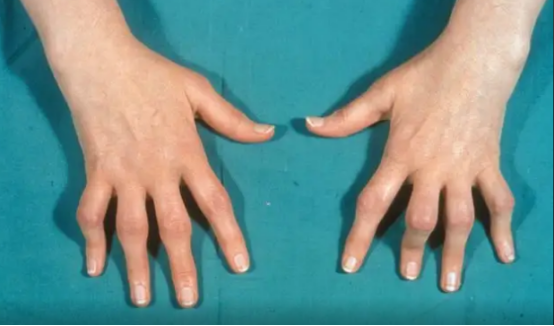
系统性疾病通过代谢紊乱和免疫异常机制促进两种疾病的发生发展。糖尿病患者因长期高血糖状态导致腱鞘滑膜糖基化产物沉积,同时降低神经组织对压迫的耐受性,使腱鞘炎与腕管综合征的发病风险分别增加 2.1 倍和 1.8 倍。甲状腺功能减退患者由于黏多糖代谢异常,易出现组织间液积聚,不仅增加腱鞘厚度,还会降低腕管的空间代偿能力。类风湿关节炎作为自身免疫性疾病的代表,其滑膜炎性反应可同时累及屈肌腱鞘和腕管滑膜组织,研究证实 RA 患者中腕管综合征的发生率是非 RA 人群的 7 倍,且此类患者的腱鞘增厚程度与类风湿因子滴度呈正相关。此外,透析患者因 β2 – 微球蛋白淀粉样沉积,腕管综合征发生率高达 5%-64%,成为特殊人群中的高发疾病。
三、病理联动:炎症扩散与生物力学失衡的恶性循环
屈指肌腱腱鞘炎与腕管综合征的关联并非简单的解剖毗邻关系,而是通过炎症扩散与生物力学失衡形成的病理联动网络。这种动态相互作用使两种疾病形成恶性循环,加速病情进展。
炎症扩散构成了二者关联的核心病理纽带。屈指肌腱腱鞘炎的局部炎症并非孤立存在,炎症因子可通过组织间隙扩散至腕管内,引发滑膜组织的继发性炎症反应。在类风湿关节炎患者中,这种炎症扩散表现得尤为典型:腱鞘炎产生的 TNF-α、IL-6 等促炎因子通过血液循环和组织间隙双重途径进入腕管,刺激滑膜细胞增生和血管翳形成。病理研究显示,此类患者的腕管滑膜厚度可达正常人群的 3-4 倍,且炎症程度与正中神经受压程度呈显著正相关。这种 “腱鞘炎 – 滑膜炎 – 神经卡压” 的炎症链,使局部病变迅速发展为区域性病理改变。
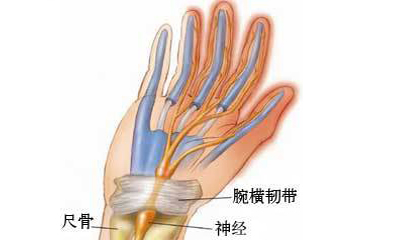
生物力学失衡则通过功能代偿机制扩大病理影响。当屈指肌腱因腱鞘炎出现滑动障碍时,机体为维持手部功能会启动代偿机制,表现为腕部过度屈曲、前臂肌肉过度收缩等异常运动模式。生物力学研究证实,这种代偿性动作可使腕管内压力瞬间升高至 80-100mmHg,远超过神经耐受阈值。一位手工编织从业者的病例显示,其因腱鞘炎导致的手指活动受限,使腕部屈曲角度增加 25°,腕管内压力较正常活动时升高 3 倍,最终诱发腕管综合征。长期异常应力不仅直接升高腕管压力,还会导致腕横韧带继发性增厚,进一步缩小腕管空间,形成 “功能障碍 – 代偿过度 – 结构改变” 的恶性循环。
神经 – 肌腱交互作用加剧了病情的复杂性。正中神经受压后出现的感觉异常和运动障碍,会导致手部精细动作控制能力下降,使屈肌腱承受更大的不均衡应力,反过来加重腱鞘炎。这种神经与肌腱之间的病理反馈,使得单纯治疗一种疾病往往效果不佳,需要采取综合干预策略。
临床诊疗:从共病识别到协同干预
屈指肌腱腱鞘炎与腕管综合征的高共病率对临床诊疗提出了特殊要求,需要建立从精准诊断到协同治疗的系统化策略。临床医生应摒弃 “见炎治炎” 的单一思维,树立整体观,重视两种疾病的关联特征。
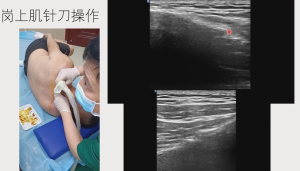
诊断方面需建立阶梯式排查流程。对主诉手指疼痛、弹响的患者,除常规检查腱鞘炎体征外,应系统询问是否存在夜间麻醒、晨僵超过 30 分钟、手部无力等神经症状。体格检查需包括 Phalen 试验、Tinel 征等神经卡压特异性检查,阳性体征提示需进一步行电生理检查。神经传导速度(NCV)和肌电图(EMG)作为金标准,可发现约 34% 的扳机指患者存在正中神经传导异常。超声检查具有双重价值,既能评估屈肌腱鞘厚度(正常<1mm,异常>2mm),又可测量正中神经横截面积(正常<10mm²,异常>13mm²),为两种疾病的共病诊断提供形态学依据。对于类风湿关节炎等高危人群,即使无明显症状,也建议每 6-12 个月进行一次超声筛查。
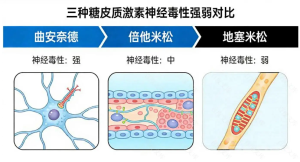
治疗策略应实现分级与协同。对轻度共病患者,可采用制动、理疗、口服非甾体抗炎药等保守治疗,同时配合腕管内局部封闭治疗(糖皮质激素 + 局麻药),研究显示其短期有效率可达 70%。对于保守治疗无效或中重度患者,需考虑手术干预,术中应同时处理增厚的腱鞘和腕横韧带,避免仅松解肌腱而忽略神经减压。糖尿病患者需注意血糖控制,因其术后愈合不良风险较高;类风湿关节炎患者则需结合免疫抑制剂治疗,以控制滑膜炎症进展。康复阶段应强调生物力学矫正,通过佩戴定制支具维持腕关节中立位,同时进行渐进性肌力训练,打破代偿性损伤的恶性循环。
预后评估需关注长期功能恢复。共病患者的康复周期通常较单一疾病延长 30%-50%,需建立长期随访机制。电生理检查的定期复查(术后 3、6、12 个月)可早期发现神经再生不良,超声监测则能评估腱鞘炎症复发情况。对于系统性疾病患者,应将手部功能评估纳入整体病情评价体系,实现原发病与并发症的协同管理。
屈指肌腱腱鞘炎与腕管综合征的关联研究揭示了人体局部病变的系统性特征。这种关联不仅体现在解剖位置的邻近,更源于病理机制的相互作用。临床医生只有深刻理解这种关联本质,才能实现从对症治疗到对因干预的提升,最终改善患者的手部功能和生活质量。